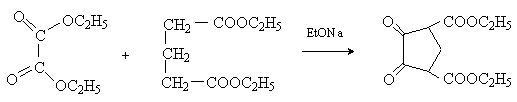Методы получения алициклических соединений.
Методы получения
Существует три основных пути синтеза алициклических соединений: 1) из ациклических соединений; 2) из ароматических и гетероциклических соединений; 3) взаимными превращениями алициклов.
К первой группе методов относятся многочисленные реакции циклизации, среди которых можно выделить следующие.
- Внутримолекулярная (реже межмолекулярная) циклизация бифункциональных соединений, которые содержат подходящим образом расположенные функциональные группы, способные взаимодействовать с образование С-С связи путем известных реакций замещения, присоединения, отщепления.
- Реакции циклоприсоединения - межмолекулярные процессы с образованием цикла из двух ненасыщенных молекул без отщепления каких либо групп или атомов, протекающие, как правило, по синхронному механизму (перициклические реакции).
- Циклоолигомеризация непредельных соединений в условиях металлокомплексного катализа.
Среди методов второй группы наибольшее значение имеет гидрирование ароматических соединений с образованием шестичленных алициклов.
Третья группа методов включает реакции расширения или сужения циклов путем перегруппировок.
Использование того или иного метода синтеза зависит прежде всего от размера цикла. Легче других образуются термодинамически устойчивые обычные циклы. Процессы их образования в результате внутримолекулярной циклизации характеризуются низкими энтальпиями активации (низкая энергия напряжения переходного состояния) и энтропиями активации (высокая вероятность образования клешневидной конформации, в которой сближены реакционные центры, участвующие в процессе циклизации). Синтез малых циклов также осуществляется достаточно легко, несмотря на их низкую термодинамическую стабильность, так как процессу циклизации благоприятствует близкое расположение реакционных центров (энтропийный фактор). Наибольшие трудности связаны с синтезом циклов среднего размера, поскольку и энтальпийный фактор (высоконапряженное переходное состояние), и энтропийный фактор (низкая вероятность сближения реакционных центров, расположенных на разных концах молекулы) не благоприятствуют циклизации.
Большинство реакций циклизации приводит к функциональным производным алициклических углеводородов (кетонам, сложным эфирам и др.), из которых они могут быть получены известными методами (восстановление, декарбоксилирование).
Малые циклы
Циклопропан.
1) Реакции 1,3-элиминирования.
1,3-Дигалогениды взаимодействуют с металлами (цинк, магний, натрий, амальгама лития) с образованием циклопропанов. Реакция представляет собой внутримолекулярный вариант синтеза Вюрца.Наилучшие результаты дает применение цинковой пыли в спирте.
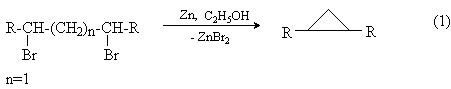
γ-Галогенкетоны, сложные эфиры и нитрилы γ -галогенкарбоновых кислот как СН-кислоты отщепляют галогеноводороды под действием сильных оснований с образованием функциональных производных циклопропана.
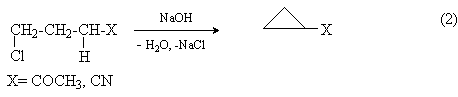
2) Циклоалкилирование 1,2-дигалогеналканами соединений с активной метиленовой группой.
1,2-Дигалогениды алкилируют натриймалоновый эфир и другие соединения с активной СН2-группой с образованием циклических продуктов диалкилирования:
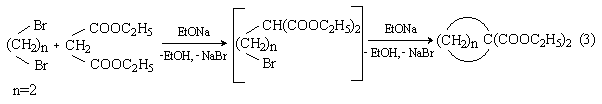
3) Реакции [2+1]-циклоприсоединения (циклопропанирование).
Карбены присоединяются по двойной связи углерод-углерод с образованием циклопропанового кольца:
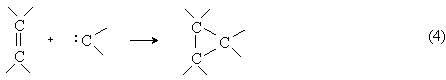
Существует несколько способов циклопропанирования, отличающихся методами генерирования карбенов:
- разложением алифатических диазосоединений в присутствии катализаторов – комплексов меди:
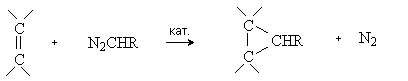
- из хлороформа под действием оснований:
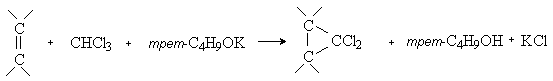
- генерированием карбеноидов из дииодметана:
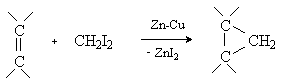
Циклобутан
1) Дегалогенирование 1,4-дигалогеналканов (схема 1, n=2).
2) Циклоалкилирование 1,3-дигалогеналканами соединений с активной метиленовой группой. (схема 3, n=3).
3) Ацилоиновая конденсация.
2-Гидроксибутанон (ацилоин) может быть получен внутримолекулярной ацилоиновой конденсацией диэтилового эфира янтарной кислоты в присутствии триметилхлорсилана:
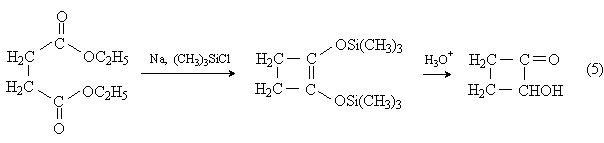
4) [2+2]-Циклоприсоединение.
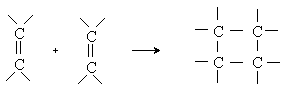
Алкены и их производные вступают в реакции циклоприсоединения с образованием циклобутанового кольца:
Реакции инициируется нагреванием или облучением:
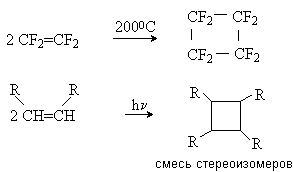
5) Электроциклические реакции 1,3-диенов.
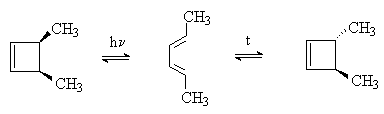
Сопряженные диены вступают в реакцию внутримолекулярной циклизации с образованием новой σ -связи по концам сопряженной системы:
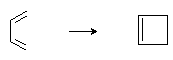
Реакция протекает по синхронному механизму и инициируется термически или фотохимически. Стереохимический результат реакции определяется правилами орбитальной симметрии и зависит от способа инициирования:
Обычные циклы
Циклогексан, циклопентан и их гомологи получают при переработке нефти (нафтены). Синтетически они могут быть получены следующими методами.
1) Восстановление аренов и ненасыщенных алициклических соединений.
Циклогексан и его гомологи получают каталитическим гидрированием бензола и гомологов бензола:
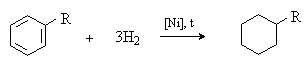
Циклопентан может быть получен гидрированием ненасыщенного алициклического углеводорода циклопентадиена (содержится в продуктах переработки каменного угля и нефти).
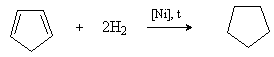
2) Дегидроциклизация алканов.
При пропускании над платиновым катализатором при 3000С алифатических углеводородов с пятью углеродными атомами в цепи происходит их дегидроциклизация с образованием циклопентана и его гомологов, например:
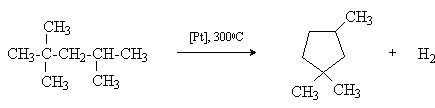
Если алкан содержит цепь из 6 и более атомов углерода, то происходит замыкание шестичленного цикла, который при отсутствии в цикле четвертичного атома углерода далее дегидрируется в бензол или его гомолог.
3) Внутримолекулярная циклизация производных дикарбоновых килот..
Обычные циклы легко образуются в результате внутримолекулярной циклизации α, ω -бифункциональных соединений, содержащих функциональные группы, способные взаимодействовать с образованием С-С связи. Такие реакции являются внутримолекулярными аналогами известных межмолекулярных реакций.
Сухая перегонка солей дикарбоновых кислот и щелочно-земельных металлов приводит к образованию циклических кетонов:
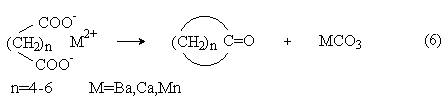
Внутримолекулярной сложноэфирной конденсацией эфиров дикарбоновых кислот (конденсация Дикмана) получают циклические кетоэфиры
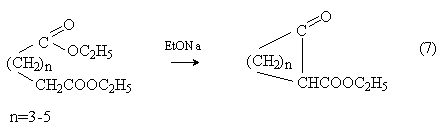
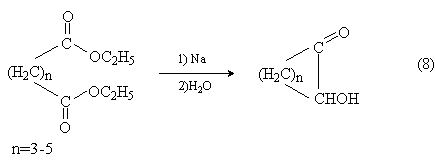
Внутримолекулярная ацилоиновая конденсация дает циклические ацилоины:
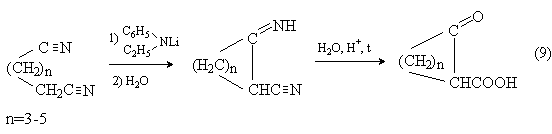
Внутримолекулярная циклизация динитрилов карбоновых кислот (метод Торпа-Циглера) приводит к иминонитрилам и далее к кетокислотам:
4) Межмолекулярная сложноэфирная конденсация.
Перекрестной сложнофирной конденсацией эфиров щавелевой (не содержит атомов водорода в α -положении и не может, следовательно, выступать в качестве метиленовой компоненты) и глутаровой кислот получают производные 1,2-циклопентандиона: