Аллены
Способы получения
- Дегалогенирование вицинальных дигалогеналкенов цинком
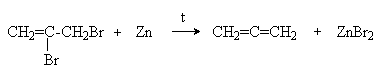
- Изомеризация алкинов
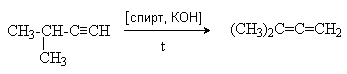
Физические свойства и структура алленов
Аллены – бесцветные газы (С3, С4) или жидкости со слабым запахом.
Углеродные атомы в молекуле аллена находятся в различных состояниях гибридизации: средний атом углерода – в sp–состоянии, два кратных – в sp2–состоянии. Поэтому p -связи, образуемые этими атомами с центральным находятся во взаимно перпендикулярных плоскостях
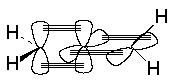
Благодаря такому строению все три атома углерода находятся на одной прямой, а заместители при крайних атомах углерода находятся во взаимно перпендикулярных плоскостях. В случае двузамещенных алленов для них возможны стереоизомеры.
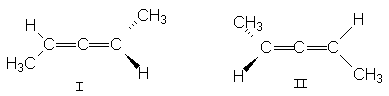
Можно видеть, что структура II является зеркальным отражением структуры I.
Реакции алленов
Аллены активны в различных реакциях, особенно в реакциях присоединения и полимеризации, однако они более реакционноспособны, чем алкены из-за напряжения, связанного с наличием двух двойных связей при центральном углеродном атоме. Наиболее типичными реакциями алленов являются:
1. Каталитическое гидрирование
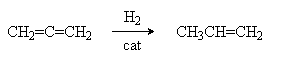
Cat: Ni, Pt, Pd
2. Изомеризация
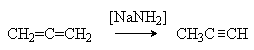
3. Циклизация
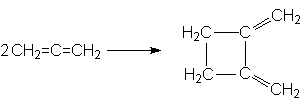
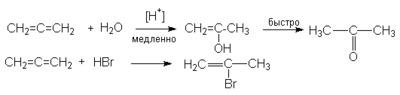
4. Реакции электрофильного присоединения
В этих реакциях центром электрофильной атаки является один из крайних атомов углерода
5. Реакции карбонилирования
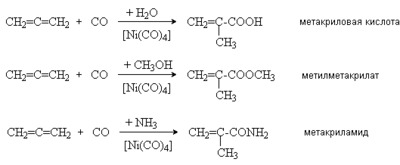
Получаемые при этом продукты используются в качестве мономеров при получении химических волокон и пластмасс.
Алкадиены с изолированными связями
Для алкадиенов этого типа характерны те же свойства, что и для алкенов, поскольку взаимное влияние двойных связей на расстоянии, более чем две С–С-связи пренебрежимо на фоне влияния ближнего структурного окружения двойной связи.
| 


