Кислотные свойства ацетилена и алкинов с терминальной тройной связью
Соединения этого типа являются С-Н – кислотами. Атом водорода, находящийся при углероде тройной связи обладает большей кислотностью, чем атом водорода алкенов и алканов. Объясняется это тем, что атомы С≡ обладают большим s-характером и поэтому сильнее притягивают электроны, поэтому С-Н связи поляризованы и электроположительные атомы водорода в них проявляют большую кислотность. Кислотность ацетилена и a -алкинов проявляется в следующих реакциях:
RC≡CH + K+NH2-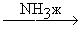 RC≡C-K+ + NH3 RC≡C-K+ + NH3
Амид-анион обладает высокой основностью, что обусловливает сдвиг равновесия в сторону образования ацетиленида. В то же время, вода, обладая более высокой кислотностью по сравнению с ацетиленом, вытесняет последний из ацетиленидов:
RC≡CК + H2O >>> RC≡CH + КOH
Натриевые, калиевые и другие ацетилениды щелочных металлов являются истинными солями, состоящие из катиона металла и ацетиленид-анионов. Соли ацетиленов с тяжелыми металлами (Ag, Cu, Hg) – не в полном смысле соли. Это ковалентно-построенные соединения, нерастворимые в воде. Они осаждаются из водного раствора.
Осаждением ацетиленида серебра определяют наличие тройной связи или отделяют терминальные ацетилены от дизамещенных:
RC≡CH + [Ag(NH3)2]NO3 >>> RC≡CAg + NH4NO3 + NH3
RC≡CR' + [Ag(NH3)2]NO3 >>> реакция не идет
Монозамещенные ацетилены тяжелых металлов легко регенерируют из осадка под действием сильных минеральных кислот.
RC≡CAg + HNO3 >>> RC≡CH + AgNO3
Аналогичное использование находят ацетилениды меди
RC≡CH + [Cu(NH3)2]Cl >>> RC≡C-Cu¯ + NH4Cl + NH3
RC≡C-Cu + HCl >>> RC≡CH + CuCl
Ацетилениды магния (реактив ) имеют важное синтетическое значение. Их получают действием терминального алкина на магний органические соединения с предельными радикалами:
RC≡CH + CH3MgI >>> CH4 + RC≡C-MgI
Благодаря этому реактиву можно получать спирты и карбоновые кислоты, содержащую тройную связь:
а) RC≡C-MgI + CH2=O >>> RC≡C-CH2-OMgI 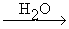 RC≡C-CH2OH + Mg(OH)I RC≡C-CH2OH + Mg(OH)I
б)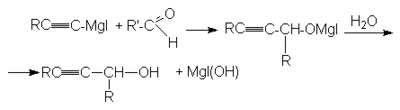
в)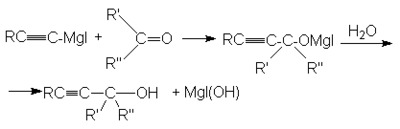
г)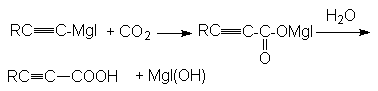
карбоновая кислота
Подобные синтезы можно осуществлять путем конденсации ацетилена или терминальных алкинов с альдегидами и кетонами (Фаворский)
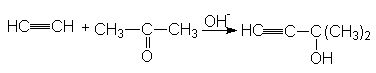
Механизм:
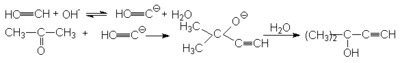 + OH- + OH-
Конденсация ацетилена с альдегидами в присутствии щелочей не дает желаемого результата из-за побочной реакции альдольной конденсации. В.Реппе осуществил ее разработав новый катализатор на основе ацетиленида меди, стабилизированного соединениями висмута:
СH≡CH + CH2O >>> CH≡CH-CH2OH 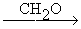 HO-CH2-C≡C-CH2-OH HO-CH2-C≡C-CH2-OH
(бутиндиол-1,4)
Изомеризация алкинов
Алкины способны к изомеризации с перемещением кратной связи или с превращением в диеновые углеводороды.
Под действие щелочных металлов тройная связь переходит на конец молекулы полученного ацетиленида. Действие спиртовых щелочей способствует переходу тройной связи с конца молекулы в центр. Промежуточными продуктами в этих превращениях являются алленовые углеводороды (Фаворский)
CH3CH2C≡CH 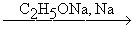 CH3C≡CCH3 CH3C≡CCH3
Окисление
RC≡CR' + KMnO4  RCOOH + R'COOH RCOOH + R'COOH
RC≡CH 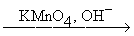 RCOOH + CO2 RCOOH + CO2
RC≡CR' 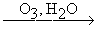 RCOOH + R'COOH RCOOH + R'COOH
Окислительная конденсация терминальных алкинов.
2RC≡CH 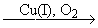 RC≡C-C≡CR RC≡C-C≡CR
Полимеризация
1) Реакция Зелинского:
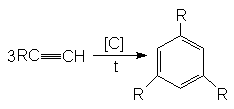
2) Димеризация:
2HC≡CH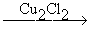 HC≡C-CH=CH2 HC≡C-CH=CH2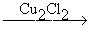 H2C=CH-C≡C-CH=CH2 H2C=CH-C≡C-CH=CH2
винилацетилен дивинилацетилен
Карбонилирование (Реппе)
CH≡CH + CO + H2O >>> CH2=CH-COOH акриловая кислота
CH≡CH + CO + ROH >>> CH2=CH-COOR эфир акриловой кислоты
CH≡CH + CO + NH3 >>> CH2=CH-CONH2 амид акриловой кислоты
Катализаторами этих реакций являются карбонилы никеля и кобальта.
| 


